Purification du sang
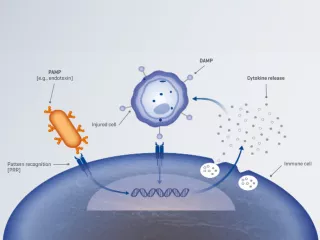
La seule thérapie capable d’éliminer efficacement les médiateurs inflammatoires, les motifs moléculaires associés aux dommages (DAMP) et/ou les motifs moléculaires associés aux pathogènes (PAMP) (p. ex., endotoxine).
Motifs moléculaires associés aux agents pathogènes (PAMP)
Tous les agents pathogènes présentent à leur surface des composants spécifiques appelés PAMP, comme les endotoxines1.
Motifs moléculaires associés aux dommages (DAMP)
Lorsque les cellules de l’hôte sont endommagées, elles libèrent des molécules endogènes appelées DAMP, comme l’adénosine triphosphate (ATP), l’acide désoxyribonucléique (ADN) mitochondrial et la protéine HMGB1 (High Mobility Group Box 1)2,3.
Médiateurs inflammatoires, comme les cytokines
Les médiateurs inflammatoires sont des molécules de signalisation essentielles qui régulent la réponse inflammatoire, notamment les cytokines pro-inflammatoires et anti-inflammatoires, comme l’interleukine (IL)-6, l’IL-8, l’IL-10 et le facteur de nécrose tumorale (TNF)-α4.
L’infection, les traumatismes, les maladies aiguës et certaines interventions thérapeutiques peuvent être associées à une réponse déséquilibrée des médiateurs inflammatoires. Les patients peuvent notamment présenter4-10 :
- Sepsis/choc septique
- COVID-19 grave
- Syndrome de détresse respiratoire aiguë (SDRA)
- Pancréatite aiguë grave
- Insuffisance hépatique aiguë et aiguë sur chronique
- Toxicité associée à la thérapie par cellules T à récepteur antigénique chimérique (CAR-T)
- Syndrome de réponse inflammatoire systémique (SRIS) causé par des brûlures graves ou un traumatisme
Le sepsis et le choc septique sont associés à des taux élevés de mortalité et de morbidité

Sepsis et choc septique
- Selon l’analyse des données de l’étude Global Burden of Diseases, le nombre annuel total de cas de sepsis et de choc septique en 2017 a été estimé à 48,9 millions, entraînant environ 11 millions de décès, soit près de 20 % de l’ensemble des décès dans le monde11.
- Des taux plasmatiques élevés de cytokines, en particulier de l’IL-6, sont associés à un risque accru de mortalité après l’admission à l’USI chez les patients atteints de sepsis ou de choc septique12-15.
- Une activité endotoxinique élevée est associée à une gravité accrue de la maladie16-18 et à une défaillance d’organe chez les patients atteints de sepsis ou de choc septique18.
Dysfonctionnement multiviscéral
- Une défaillance multiviscérale a été signalée chez environ 75 % des patients en état critique atteints de sepsis grave19
- La défaillance rénale et respiratoire combinée est fréquente chez les patients en état critique; environ 25 % des patients atteints de COVID-19 grave recevant un soutien respiratoire avancé ont également besoin d’un soutien rénal20.
- Le dysfonctionnement ou la défaillance multiviscérale peut être associé à un risque accru de mortalité à court et à long terme21-30, contribuant à jusqu’à 50 % des décès en USI21-22.
COVID-19
- En mai 2022, l’Organisation mondiale de la Santé (OMS) rapportait un total de >513 millions de cas confirmés de COVID-19 dans le monde, dont >6 millions de décès31.
- Les médiateurs inflammatoires, les DAMP et les PAMP, notamment les endotoxines et les particules du SARS-CoV-2, peuvent contribuer à la défaillance multiviscérale chez les patients atteints de COVID-19 en état critique5.
L’épuration sanguine correspond au retrait, dans le sang, de médiateurs et de toxines pouvant contribuer à la pathogenèse1,32.
Les thérapies d’épuration sanguine sont conçues pour éliminer les médiateurs inflammatoires, les PAMP (comme les endotoxines) et/ou les DAMP (comme HMGB-1) afin d’atténuer les effets d’une réponse immunitaire déséquilibrée1,33.
Les données indiquent que l’utilisation des thérapies d’épuration sanguine est associée à une diminution de la dose ou du débit de perfusion de norépinéphrine chez les patients atteints de sepsis ou de choc septique. 34-38
Une étude à répartition aléatoire, croisée et à double insu menée chez des patients en choc septique et présentant une IRA a rapporté une diminution de 87 % du débit de perfusion de norépinéphrine par rapport à la valeur de référence après 24 heures de traitement par thérapie de remplacement rénal continue (TRRC) et par thérapie d’épuration sanguine utilisant un ensemble de filtres adsorptifs conçu pour éliminer les médiateurs inflammatoires et les endotoxines (p= 0,02)38.
Les données suggèrent que l’utilisation des thérapies d’épuration sanguine est associée à une amélioration clinique de la fonction d’organe (mesurée au moyen du score SOFA) chez les patients atteints de COVID-19 sévère, avec ou sans IRA39,40.
Une étude prospective, multicentrique et observationnelle a fait état d’une amélioration de la fonction d’organe, mesurée au moyen du score Sequential Organ Failure Assessment (SOFA) (p = 0,002), chez des patients en état critique atteints de COVID-19 sévère traités par thérapie d’épuration sanguine utilisant un ensemble de filtres adsorptifs éliminant les médiateurs inflammatoires et les endotoxines (un PAMP). L’étude a également observé une mortalité réelle plus faible que la mortalité prédite selon le score Acute Physiology and Chronic Health Evaluation IV (APACHE IV)39,40.
L’épuration sanguine pourrait contribuer à atténuer la défaillance multiviscérale et à améliorer les issues cliniques34-42.
L’épuration sanguine est la seule thérapie capable d’éliminer efficacement les médiateurs inflammatoires, les DAMP et/ou les PAMP (p. ex., les endotoxines)1, ce qui peut contribuer à atténuer la défaillance multiviscérale et améliorer l’état clinique des patients34-42.
Thérapie d’épuration sanguine pour la COVID-19
Le lien entre la COVID-19 et le sepsis
Dans cet éditorial, Jean-Louis Vincent, MD, Ph. D., professeur de médecine des soins intensifs à l’Université libre de Bruxelles, explique que la COVID-19 correspond à une réponse de l’hôte dérégulée face à l’infection43.
La COVID-19 peut toucher plusieurs organes et tissus44
- Cerveau : accidents vasculaires cérébraux, convulsions, confusion mentale et inflammation cérébrale
- Yeux et nez : perte de l’odorat et conjonctivite
- Poumons : destruction de la paroi des alvéoles et diminution de l’absorption d’oxygène; toux, fièvre et dyspnée
- Cœur et vaisseaux sanguins : caillots sanguins, infarctus du myocarde et inflammation cardiaque
- Foie : taux anormaux d’enzymes
- Reins : lésions rénales pouvant résulter d’une infection virale directe des reins ou d’un choc septique
- Intestins : ≥ 20 % des patients présentent de la diarrhée
Thérapies d’épuration sanguine pour traiter les patients atteints de la COVID-19
Ce webinaire, offert par le portail d’apprentissage sur demande des Services d’apprentissage de Vantive, examine les possibilités d’utiliser des thérapies extracorporelles d’épuration sanguine chez les patients atteints de la COVID-19 présentant un dysfonctionnement d'organe.
Renseignements importants sur la sécurité
CE 0123
CE 2797
Vantive, oXiris, Prismaflex et PrisMax sont des marques de commerce de Vantive Health LLC ou de ses sociétés affiliées.
Références
-
Monard C, Rimmelé T, Ronco C. Extracorporeal blood purification therapies for sepsis. Blood Purif. 2019;47(suppl 3):1-14.
-
Gotts JE, Matthay MA. Sepsis: pathophysiology and clinical management. BMJ. 2016;353:i1585.
-
Schaefer L. Complexity of danger: the diverse nature of damage-associated molecular patterns. J Biol Chem. 2014;289(51):35237-35245.
-
Singer M, Deutschman CS, Seymour CW, et al. The third international consensus definitions for sepsis and septic shock (Sepsis-3). JAMA. 2016;315(8):801-810.
-
Nadim MK, Forni LG, Mehta RL, et al. COVID-19-associated acute kidney injury: consensus report of the 25th Acute Disease Quality Initiative (ADQI) Workgroup. Nat Rev Nephrol. 2020;16(12):747-764.
-
Husain-Syed F, Slutsky AS, Ronco C. Lung-kidney cross-talk in the critically ill patient. Am J Respir Crit Care Med. 2016;194(4):402-414.
-
Shen Y, Cui N, Miao B, et al. Immune dysregulation in patients with severe acute pancreatitis. Inflammation. 2011;34:36-42.
-
Ilonen I, Koivusalo AM, Repo H, Höckerstedt K, Isoniemi H. Cytokine profiles in acute liver failure treated with albumin dialysis. Artif Organs. 2008;32(1):52-60.
-
Shimabukuro-Vornhagen A, Gödel P, Subklewe M, et al. Cytokine release syndrome. J Immunother Cancer. 2018;6:56.
-
Jeschke MG, van Baar ME, Choudhry MA, Chung KK, Gibran NS, Logsetty S. Burn injury. Nat Rev Dis Primers. 2020;6(1):11.
-
Rudd KE, Johnson SC, Agesa KM, et al. Global, regional, and national sepsis incidence and mortality, 1990-2017: analysis for the Global Burden of Disease Study. Lancet. 2020;395(10219):200-211.
-
Andaluz-Ojeda D, Bobillo F, Iglesias V, et al. A combined score of pro- and anti-inflammatory interleukins improves mortality prediction in severe sepsis. Cytokine. 2012;57(3):332-336.
-
Mat-Nor MB, Md Ralib A, Abdulah NZ, Pickering JW. The diagnostic ability of procalcitonin and interleukin-6 to differentiate infectious from noninfectious systemic inflammatory response syndrome and to predict mortality. J Crit Care. 2016;33:245-251.
-
Barre M, Behnes M, Hamed S, et al. Revisiting the prognostic value of monocyte chemotactic protein 1 and interleukin-6 in the sepsis-3 era. J Crit Care. 2018;43:21-28.
-
Bozza FA, Salluh JI, Japiassu AM, et al. Cytokine profiles as markers of disease severity in sepsis: a multiplex analysis. Crit Care. 2007;11(2):R49.
-
Biagioni E, Venturelli C, Klein DJ, et al. Endotoxin activity levels as a prediction tool for risk of deterioration in patients with sepsis not admitted to the intensive care unit: a pilot observational study. J Crit Care. 2013;28(5):612-617.
-
Ikeda T, Ikeda K, Suda S, et al.Usefulness of the endotoxin activity assay as a biomarker to assess the severity of endotoxemia in critically ill patients. Innate Immun. 2014;20:881-887.
-
Ikeda T, Kamohara H, Suda S, et al. Comparative evaluation of endotoxin activity level and various biomarkers for infection and outcome of icu-admitted patients. Biomedicines. 2019;7:47.
-
Blanco J, Muriel-Bombín A, Sagredo V, et al. Incidence, organ dysfunction and mortality in severe sepsis: a Spanish multicentre study. Crit Care. 2008;12(6):R158. doi:10.1186/cc7157.
-
ICNARC. ICNARC report on COVID-19 in critical care: England, Wales and Northern Ireland 08 April 2022. Accessed April 2022. Available at: https://www.icnarc.org/our-audit/audits/cmp/reports
-
Mayr VD, Dünser MW, Greil V, et al. Causes of death and determinants of outcome in critically ill patients. Crit Care. 2006;10(6):R154.
-
Orban JC, Walrave Y, Mongardon N, et al. Causes and characteristics of death in intensive care units: a prospective multicenter study. Anesthesiology. 2017;126(5):882-889.
-
Lie KC, Lau C, Chau NV, et al. Utility of SOFA score, management and outcomes of sepsis in Southeast Asia: a multinational multicenter prospective observational study. J Int Care. 2018;6:9.
-
Lone NI, Walsh TS.Impact of intensive care unit organ failures on mortality during the five years after a critical illness. Am J Respir Crit Care Med. 2012;186:640-647.
-
Jain A, Palta S, Saroa R, Palta A, Sama S, Gombar S. Sequential organ failure assessment scoring and prediction of patient's outcome in intensive care unit of a tertiary care hospital. J Anaesthesiol Clin Pharmacol. 2016;32(3):364-368.
-
Ferreira FL, Bota DP, Bross A, Mélot C, Vincent JL. Serial evaluation of the SOFA score to predict outcome in critically ill patients. JAMA. 2001;286(14):1754-1758.
-
Liu J, Zhang S, Wu Z, et al. Clinical outcomes of COVID-19 in Wuhan, China: a large cohort study. Ann Intensive Care. 2020;10:99.
-
Jin M, Lu Z, Zhang X, et al. Clinical characteristics and risk factors of fatal patients with COVID-19: a retrospective cohort study in Wuhan, China. BMC Infect Dis. 2021;21:951.
-
Zhou F, Yu T, Du R, et al. Clinical course and risk factors for mortality of adult inpatients with COVID-19 in Wuhan, China: a retrospective cohort study. Lancet. 2020;395(10229):1054-1062.
-
Juvé-Udina ME, Adamuz J, López-Jimenez MM, et al. Predicting patient acuity according to their main problem. J Nurs Manag. 2019;27(8):1845-1858.
-
WHO COVID-19 Dashboard. 2022. Accessed May 2022. Available at: https://www.covid19.who.int.
-
Rimmelé T, Kellum JA. Clinical review: blood purification for sepsis. Crit Care. 2011;15(1):205.
-
Malard B, Lambert C, Kellum JA. In vitro comparison of the adsorption of inflammatory mediators by blood purification devices. Intensive Care Med Exp. 2018;6(1):12.
-
Turani F, Barchetta R, Falco M, Busatti S, Weltertet L. Continuous renal replacement therapy with the adsorbing filter Oxiris in septic patients: a case series. Blood Purif. 2019;47(suppl 3):54-58.
-
Schwindenhammer V, Girardot T, Chaulier K, et al. oXiris® use in septic shock: experience of two french centres. Blood Purif. 2019;47:29-35.
-
Lumlertgul N, Srisawat N. The haemodynamic effects of Oxiris haemofilter in septic shock patients requiring renal support: a single-centre experience. Int J Artif Organs. 2020;44:17-24.
-
Hawchar F, László I, Öveges N, Trásy D, Ondrik Z, Molnar Z. Extracorporeal cytokine adsorption in septic shock: a proof of concept randomized, controlled pilot study. J Crit Care. 2019;49:172-178.
-
Broman ME, Hansson F, Vincent JL, Bodelsson M. Endotoxin and cytokine reducing properties of the Oxiris membrane in patients with septic shock: a randomized crossover double-blind study. PLoS One. 2019;14:e0220444.
-
Villa G, Romagnoli S, De Rosa S, et al. Blood purification therapy with a hemodiafilter featuring enhanced adsorptive properties for cytokine removal in patients presenting COVID-19: a pilot study. Crit Care. 2020;24:605.
-
Nassiri AA, Hakemi MS, Miri MM, Shahrami R, Koomleh AA, Sabaghian T. Blood purification with CytoSorb in critically ill COVID-19 patients: a case series of 26 patients. Artif Organs. 2021;45(11):1338-1347.
-
Cruz DN, Antonelli M, Fumagalli R, et al. Early use of polymyxin B hemoperfusion in abdominal septic shock: the EUPHAS randomized controlled trial. JAMA. 2009;301(23):2445-52.
-
Rosalia RA, Ugurov P, Neziri D, et al. Extracorporeal blood purification in moderate and severe COVID-19 patients: a prospective cohort study. Blood Purif. 2022;51:233-242.
-
Vincent JL. COVID-19: it's all about sepsis. Future Microbiol. 2021;16:131-133.
-
Wadman M, Couzin-Frankel J, Kaiser J, Matacicet C. A rampage through the body. Science. April 17, 2020. Accessed April 2020. Available at: https://www.science.org/content/article/how-does-coronavirus-kill-clinicians-trace-ferocious-rampage-through-body-brain-toes.