Thérapie de remplacement rénal continu (TRRC)
Insuffisance rénale aiguë : chaque patient est différent
L’insuffisance rénale aiguë (IRA) est définie comme une diminution soudaine de la fonction rénale survenant en 7 jours ou moins, englobant à la fois une atteinte directe du rein et une altération aiguë de sa fonction8.
L’IRA est un syndrome hétérogène8,9 associé à de mauvais résultats cliniques, chaque patient présentant un profil de risque et une trajectoire d’évolution de la maladie qui lui sont propres10,11 .
Les incidences rapportées varient
L’incidence déclarée de l’IRA chez les patients en unité de soins intensifs (USI) varie de 0,5 % à 78,7 %12-14; jusqu’à environ 25 % de ces patients peuvent nécessiter une thérapie de remplacement rénal (TRR)15-18.
Risque de mortalité
L’IRA est associée à un risque accru de morbidité19-29 ainsi qu’à une mortalité à court et à long terme30-35.
Progression vers une MRC
L’IRA est associée à un risque accru de progression vers une maladie rénale chronique (MRC), y compris une insuffisance rénale terminale (IRT)31,34,36.
État hémodynamique
De nombreux cliniciens privilégient la TRRC plutôt que la TRRI pour les patients atteints d’IRA qui présentent une instabilité hémodynamique6,36,37.
Gravité de la surcharge hydrique
Les lignes directrices cliniques recommandent la TRRC chez les patients présentant une pression intracrânienne élevée ou un œdème cérébral généralisé causé par une surcharge hydrique6.
Nous suggérons d’utiliser la TRRC plutôt que la TRRI chez les patients présentant une instabilité hémodynamique. (Grade 2B)6
KDIGO Clinical Practice Guideline for Acute Kidney Injury
La TRRC est la modalité de TRR privilégiée pour les patients atteints d’IRA qui nécessitent une gestion précise des liquides ou qui présentent une instabilité hémodynamique.
TRRC pour une gestion précise des liquides
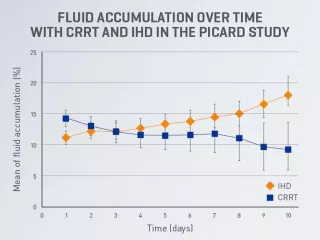
Il a été démontré que la TRRC réduit efficacement et rapidement l’accumulation de liquides37,38, tout en offrant la flexibilité d’ajuster à tout moment l’intensité du retrait de liquide selon l’évolution de l’état clinique du patient6.
Les données disponibles suggèrent que la TRRC pourrait offrir un meilleur contrôle de la gestion des liquides que d’autres modalités de TRR6,38-40 .
Figure adaptée de Bouchard J et al. Kidney Int. 2009;76(4):455-427. Les détails sur la collecte des données et l’analyse statistique n’ont pas été rapportés.
TRRC pour les patients atteints d’IRA présentant une instabilité hémodynamique
L’instabilité hémodynamique est fréquente chez les patients en état critique atteints d’IRA recevant une TRR (~36 à 70 % des patients)40,41, et pourrait être associée à un risque accru de mortalité et de progression de l’IRA. 42,43
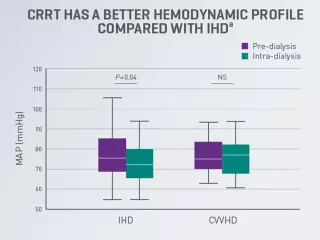
Les données médicales existantes suggèrent que la TRRC pourrait mieux maintenir la stabilité hémodynamique tout en retirant du liquide, comparativement à l’hémodialyse intermittente (HDI) et à la dialyse continue à faible intensité (SLED)38,44-46.
aEssai contrôlé à répartition aléatoire portant sur 80 patients adultes en état critique présentant une insuffisance rénale aiguë nécessitant une dialyse dans les USI d’un établissement aux États-Unis (1995-1999). Les données portent sur l’HDI et l’hémodialyse veino-veineuse continue (HDVVC) durant la première journée de dialyse. Les valeurs médianes sont présentées avec l’intervalle interquartile (bords de la boîte) et les valeurs extrêmes (moustaches)38.
La TRRC peut constituer une thérapie rentable offrant des avantages cliniques et opérationnels supplémentaires pour les patients et les établissements hospitaliers.
Rentabilité de la TRRC
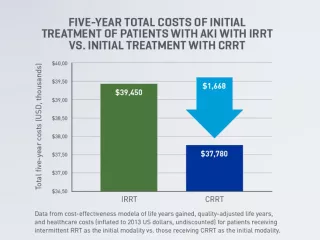
Le traitement initial des patients atteints d’IRA au moyen de la TRRC pourrait être plus rentable cinq ans après le début de la TRR que d’autres modalités de TRR3. Une analyse de rentabilité a estimé que la TRRC pourrait permettre une économie d’environ 1 668 $ sur cinq ans (selon le dollar américain de 2013)3,b,c.
Les analyses de rentabilité indiquent que la TRRC est plus rentable que la TRRI, le taux de dépendance à la dialyse étant le principal facteur influençant la rentabilité47.
bModèle des années de vie gagnées, des années de vie ajustées en fonction de la qualité et des coûts de soins de santé (rajustés selon le dollar américain de 2013, non actualisés) pour les patients recevant la TRR intermittente comme modalité initiale comparativement à ceux recevant la TRRC comme modalité initiale. Pour la TRRC initiale comme pour la TRR intermittente, la proportion dépendante du temps de patients survivants à une IRA devenant dépendants de la dialyse a été établie d’après l’étude de Wald et al. (Crit Care Med. 2014; 42:868–877).3
cLe modèle d’analyse coût-efficacité prenait uniquement en compte le coût de mise en œuvre de la TRRC ou de la TRR intermittente à l’USI, le coût quotidien de l’indépendance à la dialyse et le coût quotidien de la dépendance à la dialyse en consultation externe3.
Avantages d’un système intégré de soutien d’organes
La TRRC peut être combinée à d’autres thérapies de soutien d’organes sur une plateforme unique, permettant une prise en charge intégrée des patients présentant une défaillance multiviscérale37.
Un rapport de consensus du 17e groupe de travail de l’ Acute Disease Quality Initiative (ADQI) indique que « dans les situations où d’autres thérapies extracorporelles sont nécessaires, la TRRC est recommandée et les systèmes intégrés sont préférés aux systèmes parallèles »37.
Épisode 1 : Décider quand et chez qui amorcer une dialyse aiguë : Des données probantes à la pratique clinique
Animé par Ravi Mehta, UC San Diego, avec Marlies Ostermann, Guy’s and St. Thomas’ Foundation Trust
Épisode 2 : Prolonger la durée de vie du filtre pendant la TRRC : Pratiques exemplaires en matière d’anticoagulation et d’utilisation du citrate
Animé par Ravi Mehta, UC San Diego, avec Ashita Tolwani, University of Alabama at Birmingham
Épisode 3 : Comment créer un programme de qualité des soins en dialyse aiguë : Indicateurs de qualité et amélioration continue
Animé par Ravi Mehta, UC San Diego, avec Theresa Mottes, Baylor College of Medicine
Renseignements importants sur la sécurité
Pour une utilisation sûre et adéquate des dispositifs, veuillez consulter le mode d’emploi.
PrisMax :
- Le moniteur PrisMax est conçu pour : La thérapie de remplacement rénal continu (TRRC) pour les patients qui souffrent d’insuffisance rénale aiguë et/ou de surcharge liquidienne.
- Les échanges plasmatiques thérapeutiques (EPT) pour les patients atteints de maladies pour lesquelles l’élimination de composants du plasma est indiquée.
- L’hémoperfusion (HP) pour les patients souffrant de troubles pour lesquels l’élimination immédiate des substances par absorption est indiquée.
Tous les traitements administrés par le biais du moniteur PrisMax doivent être prescrits par un médecin.
AVERTISSEMENT!
Utiliser uniquement des solutions conçues pour l’administration intraveineuse et approuvées pour la TRRC, l’EPT ou l’HP. Ne pas utiliser de solutions destinées à d’autres usages, comme l’alimentation entérale, les lipides ou les médicaments cytotoxiques.
CONTRE-INDICATIONS
Il n’y a pas de contre-indication absolue connue aux thérapies de remplacement rénal continu.
Il n’y a pas de contre-indication connue aux thérapies d'échanges plasmatiques.
Il n’y a pas de contre-indication connue à l’hémoperfusion.
L’anticoagulation régionale au citrate est contre-indiquée chez les patients souffrant d’une insuffisance hépatique grave et d’un état de choc avec hypoperfusion musculaire.
Dans les cas suivants, le médecin traitant doit évaluer soigneusement le rapport bénéfice/risque du patient (contre-indications relatives).
- Impossibilité d’établir un accès vasculaire.
- Instabilité hémodynamique grave.
- Hypersensibilité connue à tout composant du système jetable Prismaflex.
Références
-
Ostermann M, Joannidis M, Pani A, et al. Patient selection and timing of continuous renal replacement therapy. Blood Purif. 2016;42(3):224-237.
-
Acute Dialysis Quality Initiative (ADQI) 17 Workgroup. ADQI 17 Figures. 2016. Accessed July 8, 2024. https://pittccmblob.blob.core.windows.net/adqi/17fig.pdf
-
Koyner JL, Mackey RH, Echeverri J, et al. Dialysis dependence at 90 days post discharge for patients treated with continuous renal replacement therapy (CRRT) vs. intermittent hemodialysis (IHD). Poster presented at: 28th International Conference on Advances in Critical Care Nephrology – AKI & CRRT 2023; March 29 - April 1, 2023; San Diego, California, USA.
-
Naorungroj T, Neto AS, Wang A, Gallagher M, Bellomo R. Renal outcomes according to renal replacement therapy modality and treatment protocol in the ATN and RENAL trials. Crit Care. 2022;26:269.
-
Ethgen O, Schneider AG, Bagshaw SM, Bellomo R, Kellum JA. Economics of dialysis dependence following renal replacement therapy for critically ill acute kidney injury patients. Nephrol Dial Transplant. 2015;30(1):54-61.
-
Wald R, Gaudry S, da Costa BR, et al. Initiation of continuous renal replacement therapy versus intermittent hemodialysis in critically ill patients with severe acute kidney injury: a secondary analysis of STARRT-AKI trial. Intensive Care Med. 2023;49(11):1305-1316.
-
Ethgen O, Murugan R, Echeverri J, Blackowicz M, Harenski K, Ostermann M. Economic analysis of renal replacement therapy modality in acute kidney injury patients with fluid overload. Crit Care Explor. 2023;5(6):e0921.
-
KDIGO Acute Kidney Injury Work Group. KDIGO Clinical Practice Guideline for Acute Kidney Injury. Kidney Int Suppl. 2012;2(1):1-138.
-
Aglae C, Muller L, Reboul P, et al. Heterogeneity of cause, care, and prognosis in severe acute kidney injury in hospitalized patients: a prospective observational study. Can J Kidney Health Dis. 2019;6.
-
Cerdá J, Lameire N, Eggers P, et al. Epidemiology of acute kidney injury. Clin J Am Soc Nephrol. 2008;3(3):881-886.
-
Kellum JA, Sileanu FE, Bihorac A, Hoste EA, Chawla LS. Recovery after acute kidney injury. Am J Respir Crit Care Med. 2017;195(6):784-791.
-
Chawla L, Bellomo R, Bihorac A, et al. Acute kidney disease and renal recovery: consensus report of the Acute Disease Quality Initiative (ADQI) 16 Workgroup. Nat Rev Nephrol. 2017;13:241-257.
-
Mehta S, Chauhan K, Patel A, et al. The prognostic importance of duration of AKI: a systematic review and meta-analysis. BMC Nephrol. 2018;19(1):91.
-
Nisula S, Kaukonen KM, Vaara ST, et al. Incidence, risk factors and 90-day mortality of patients with acute kidney injury in Finnish intensive care units: the FINNAKI study. Intensive Care Med. 2013;39:420-428.
-
Melo FAF, Macedo E, Fonseca Bezerra AC, et al. A systematic review and meta-analysis of acute kidney injury in the intensive care units of developed and developing countries. PLoS One. 2020;15(1):e0226325.
-
Jiang L, Zhu Y, Luo X, et al. Epidemiology of acute kidney injury in intensive care units in Beijing: the multi-center BAKIT study. BMC Nephrol. 2019;20:468.
-
Bouchard J, Acharya A, Cerda J, et al. A prospective international multicenter study of AKI in the intensive care unit. Clin J Am Soc Nephrol. 2015;10(8):1324-1331.
-
Uchino S, Kellum JA, Bellomo R, et al. Acute renal failure in critically ill patients: a multinational, multicenter study. JAMA. 2005;294(7):813-818.
-
De Corte W, Dhondt A, Vanholder R, et al. Long-term outcome in ICU patients with acute kidney injury treated with renal replacement therapy: a prospective cohort study. Crit Care. 2016;20:256.
-
Garzotto F, Ostermann M, Martín-Langerwerf D, et al. The Dose Response Multicentre Investigation on Fluid Assessment (DoReMIFA) in critically ill patients. Crit Care. 2016; 20:196.
-
Gammelager H, Christiansen CF, Johansen MB, Tønnesen E, Jespersen B, Sørensen HT. Three-year risk of cardiovascular disease among intensive care patients with acute kidney injury: a population-based cohort study. Crit Care. 2014;18(5):492.
-
Go AS, Hsu C, Yang JT, et al. Acute kidney injury and risk of heart failure and atherosclerotic events. Clin J Am Soc Nephrol. 2018;13(6):833-841.
-
Wu V, Wu C, Huang T, et al. Long-term risk of coronary events after AKI. J Am Soc Nephrol. 2014;25(3):595-605.
-
Wu VC, Wu PC, Wu CH, et al. The impact of acute kidney injury on the long-term risk of stroke. J Am Heart Assoc. 2014;3(4):e000933.
-
Brown JR, Parikh C, Ross C, et al. Impact of perioperative acute kidney injury as a severity index for thirty-day readmission after cardiac surgery. Ann Thorac Surg. 2014;97(1)111-117.
-
Brown JR, Hisey W, Marshall E, et al. Acute kidney injury severity and long-term readmission and mortality after cardiac surgery. Ann Thorac Surg. 2016;102(5):1482-1489.
-
Lai TS, Wang CY, Pan SC, et al. Risk of developing severe sepsis after acute kidney injury: a population-based cohort study. Crit Care. 2013;17:R231.
-
Horkan CM, Purtle SW, Mendu ML, Moromizato T, Gibbons FK, Christopher KB. The association of acute kidney injury in the critically ill and postdischarge outcomes: a cohort study. Crit Care Med. 2015;43(2):354-364.
-
Koulouridis I, Price LL, Madias NE, Jaber BL. Hospital-acquired acute kidney injury and hospital readmission: a cohort study. Am. J. Kidney Dis. 2015;65(2)275-282.
-
Sawhney S, Marks A, Fluck N, et al. Acute kidney injury as an independent risk factor for unplanned 90-day hospital readmissions. BMC Nephrol. 2017;18:9.
-
Silver SA, Harel Z, McArthur E, et al. 30-day readmissions after an acute kidney injury hospitalization. Am J Med. 2017;130(2)163-172.
-
Coca SG, Yusuf B, Shlipak MG, Garg AX, Parikh CR. Long-term risk of mortality and other adverse outcomes after acute kidney injury: a systematic review and meta-analysis. Am J Kidney Dis. 2009; 53(6):961-973.
-
See EJ, Jayasinghe K, Glassford N, et al. Long-term risk of adverse outcomes after acute kidney injury: a systematic review and meta-analysis of cohort studies using consensus definitions of exposure. Kidney Int. 2019;95(1):160-172.
-
Srisawat N, Sileanu FE, Murugan R, et al. Variation in risk and mortality of acute kidney injury in critically ill patients: a multicenter study. Am J Nephrol. 2015;41(1):81-88.
-
Hoste EA, Bagshaw SM, Bellomo R, et al. Epidemiology of acute kidney injury in critically ill patients: the multinational AKI-EPI study. Intensive Care Med. 2015;41(8):1411-1423.
-
Coca SG, Singanamala S, Parikh CR. Chronic kidney disease after acute kidney injury: a systematic review and meta-analysis. Kidney Int. 2012;81(5):442-448.
-
Ronco C, Ricci Z, De Backer D, et al. Renal replacement therapy in acute kidney injury: controversy and consensus. Crit Care. 2015;19(1):146.
-
Nadim MK, Forni LG, Bihorac A, et al. Cardiac and vascular surgery-associated acute kidney injury: the 20th international consensus conference of the ADQI (Acute Disease Quality Initiative) group. J Am Heart Assoc. 2018;7(11):e008834.
-
Augustine JJ, Sandy D, Seifert TH, Paganini EP. A randomized controlled trial comparing intermittent with continuous dialysis in patients with ARF. Am J Kidney Dis. 2004;44(6):1000-1007.
-
Bouchard J, Soroko SB, Chertow GM, et al. Fluid accumulation, survival and recovery of kidney function in critically ill patients with acute kidney injury. Kidney Int. 2009;76(4):422-427.
-
Clark WR, Ding X, Qiu H, et al. Renal replacement therapy practices for patients with acute kidney injury in China. PLoS One. 2017;12(7):e0178509.
-
STARRT-AKI Investigators; Canadian Critical Care Trials Group; Australian and New Zealand Intensive Care Society Clinical Trials Group. Timing of initiation of renal-replacement therapy in acute kidney injury. N Engl J Med. 2020;383(5):502.
-
Izawa J, Kitamura T, Iwami T, et al. Early-phase cumulative hypotension duration and severe-stage progression in oliguric acute kidney injury with and without sepsis: an observational study. Crit Care. 2016;20:405.
-
Haase-Fielitz A, Haase M, Bellomo R, et al. Perioperative hemodynamic instability and fluid overload are associated with increasing acute kidney injury severity and worse outcome after cardiac surgery. Blood Purif. 2017;43(4):298-308.
-
Bagshaw SM, Berthiaume LR, Delaney A, Bellomo R. Continuous versus intermittent renal replacement therapy for critically ill patients with acute kidney injury: a meta-analysis. Crit Care Med. 2008;36(2):610-617.
-
Fieghen HE, Friedrich JO, Burns KE, et al. The hemodynamic tolerability and feasibility of sustained low efficiency dialysis in the management of critically ill patients with acute kidney injury. BMC Nephrol. 2010;11:32.
-
Singh A, Hussain S, Kher V, Palmer AJ, Jose M, Antony B. A systematic review of cost-effectiveness analyses of continuous versus intermittent renal replacement therapy in acute kidney injury. Expert Rev Pharmacoecon Outcomes Res. 2022;22(1):27-35.